- Szerző Rachel Wainwright wainwright@abchealthonline.com.
- Public 2023-12-15 07:40.
- Utoljára módosítva 2025-11-02 20:14.
Avastin
Avastin: használati utasítás és vélemények
- 1. Kiadási forma és összetétel
- 2. Farmakológiai tulajdonságok
- 3. Felhasználási javallatok
- 4. Ellenjavallatok
- 5. Az alkalmazás módja és adagolása
- 6. Mellékhatások
- 7. Túladagolás
- 8. Különleges utasítások
- 9. Alkalmazás terhesség és szoptatás alatt
- 10. Használja idős korban
- 11. Gyógyszerkölcsönhatások
- 12. Analógok
- 13. A tárolás feltételei
- 14. A gyógyszertárakból történő kiadás feltételei
- 15. Vélemények
- 16. Ár gyógyszertárakban
Latin neve: Avastin
ATX kód: L01XC07
Hatóanyag: Bevacizumab (Bevacizumab)
Gyártó: F. Hoffmann-La Roche Ltd. (Svájc), Roche Diagnostics (Németország), Genentech Inc. (USA)
Leírás és fotófrissítés: 2019.09.16
Árak a gyógyszertárakban: 8755 rubeltől.
megvesz
Az Avastin daganatellenes szer, amely monoklonális antitestekhez tartozik. A gyógyszer alkalmazása segít elnyomni a betegség metasztatikus előrehaladását és csökkenteni a mikrovaszkuláris permeabilitást különböző típusú daganatokban (emlő-, prosztata-, hasnyálmirigy-, vastagbélrák).
Kiadási forma és összetétel
Az Avastin koncentrátum formájában kapható infúziós oldat elkészítéséhez, lehet világosbarna színű vagy színtelen.
A gyógyszer hatóanyaga a bevacizumab.
Ez a gyógyszer 100 mg / 4 ml és 400 mg / 16 ml bevazumab csomagolásban kapható.
Farmakológiai tulajdonságok
Farmakodinamika
Az Avastin egy humanizált rekombináns hiperkimer monoklonális antitest, amely szelektíven kötődik és semlegesíti a vaszkuláris endoteliális növekedési faktort (VEGF), amelynek biológiai aktivitása van. A bevacizumab, a gyógyszer aktív komponense, gátolja az érrendszeri endothel növekedési faktor kötődését az endothelsejtek felszínén elhelyezkedő 1. és 2. típusú receptorokhoz (Flt-1, KDR). Ez a vaszkularizáció csökkenéséhez és a tumor növekedésének elnyomásához vezet.
A bevacizumab teljesen humán vázrégiókat tartalmaz, az egér hiperkimer antitestjének komplementaritást meghatározó régióival, amelyek kötődnek a VEGF-hez. Ezt a vegyületet rekombináns DNS-technológiával állítják elő egy kínai hörcsög petefészek expressziós rendszerben. A bevacizumab hossza 214 aminosav, molekulatömege hozzávetőlegesen 149 000 dalton.
Az Avastin bevezetése gátolja a betegség metasztatikus előrehaladását, és csökkenti a mikrovaszkuláris permeabilitást különböző emberi rákos megbetegedésekben, beleértve a prosztata mirigy, hasnyálmirigy, emlő és vastagbél rákját is.
A bevacizumab karcinogén és mutagén potenciálja nem jól ismert. Állatoknak történő beadáskor rögzítették a testre gyakorolt embriotoxikus és teratogén hatásokat. A gyógyszer alkalmazását az aktív növekedési szakaszba lépő és nyitott növekedési zónákkal rendelkező állatoknál gyakran a porcos lemez dysplasia kísérte.
Farmakokinetika
A bevacizumab farmakokinetikája kétkamrás modell segítségével írható le. Az anyag eloszlását alacsony clearance, alacsony eloszlási térfogat és a központi kamra hosszú felezési ideje jellemzi, amely lehetővé teszi az Avastin szükséges terápiás plazmakoncentrációjának fenntartását az infúzió során 2-3 hetente egyszer.
A bevacizumab clearance-e nem függ a beteg életkorától. Szintén 30% -kal magasabb az alacsony albuminszinttel rendelkező betegeknél, és 7% -kal magasabb a jelentős daganattömegű betegeknél, összehasonlítva az átlagos albumin-koncentrációval és tumor-tömegértékekkel rendelkező betegeknél.
Az eloszlási térfogat 3,28 liter, illetve 2,73 liter férfi, illetve nő esetében, ami megfelel a G osztályú immunglobulinok (IgG) és más monoklonális antitestek eloszlási térfogatának. Az elosztási térfogat a perifériás kamrában eléri a férfiaknál és a nőknél a 2,35 litert, míg a nőknél az 1,69 litert, ha az Avastint más rákellenes gyógyszerekkel kombinálják. Férfi betegek testtömeg-adagjának módosítása után az eloszlás térfogata 20% -kal nagyobb, mint a nőknél.
A 125 I-bevacizumab egyszeri intravénás beadása után metabolikus jellemzői megegyeznek egy természetes IgG molekula jellemzőivel, amely nem kötődik a VEGF-hez. Az Avastin aktív komponensének metabolizmusa és kiválasztása teljes mértékben megfelel az endogén IgG metabolizmusának és kiválasztásának, vagyis főleg proteolitikus katabolizmus útján végzik a test minden sejtjében, beleértve az endothel sejteket is, és nem a májon és a vesén keresztül. Az IgG az újszülött receptoraihoz kötődik az IgG kristályosodó fragmenseihez (FcRn receptorok), amely eltávolítja a sejtanyagcsere folyamataiból és hosszú felezési időt biztosít.
A bevacizumab farmakokinetikája lineáris a heti 1,5-10 mg / kg dózisok között. Ennek a vegyületnek a clearance-e férfiaknál 0,22 l / nap, nőknél 0,188 l / nap. A dózis testtömeg-kiigazítását követően a bevacizumab clearance-e férfiaknál 17% -kal nő a női betegekhez képest. Az anyag felezési ideje férfiaknál 20 nap, nőknél - 18 nap.
A bevacizumab farmakokinetikája nem függ a beteg életkorától. Gyermekeknél és serdülőknél alkalmazott anyag farmakokinetikájára vonatkozó adatok korlátozottak. A rendelkezésre álló adatok azt bizonyítják, hogy nincs különbség a bevacizumab clearance-e és megoszlási térfogata között gyermekeknél, serdülőknél és jelentős daganatos felnőtt betegeknél. Az Avastin hatékonyságát és biztonságosságát máj- és / vagy veseelégtelenségben szenvedő betegeknél kevéssé vizsgálták, mivel a vese és a máj nem azok a fő szervek, amelyekben a bevacizumab metabolizmusa és az azt követő kiválasztása zajlik.
Felhasználási indikációk
Az utasítások szerint az Avastint a következőkre írják fel:
- Metasztatikus vagy lokálisan visszatérő emlőrák;
- Előrehaladott, működésképtelen metasztatikus vagy visszatérő nem laphámsejtes, nem kissejtes tüdőrák;
- Előrehaladott és / vagy áttétes vesesejtes karcinóma;
- Metasztatikus vastagbélrák;
- Ismétlődő glioblastoma.
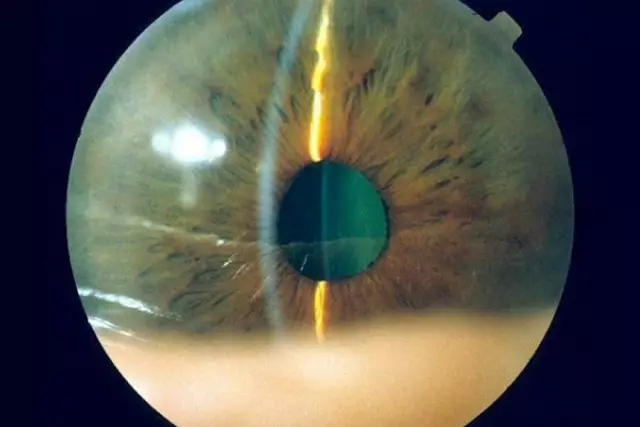
Az Avastin szemészeti alkalmazásának oka az életkorral összefüggő makula degeneráció, macula ödéma, a peri-macula régió daganatai, a diabéteszes retinopathia és néhány más, az erek kóros növekedésével összefüggő szembetegség nedves formájának kezelése. Az üvegtestbe történő injekciók eredményei bizonyítják ennek az eljárásnak a hatékonyságát és jó tolerálhatóságát proliferatív diabéteszes retinopathiában szenvedő betegeknél. Az Avastin szemészeti alkalmazásának célja a szubretinális neovaszkuláris membrán stabilizálása. A gyógyszer üvegtestbe történő befecskendezésének mellékhatásai minimálisak.
Ellenjavallatok
Az Avastin nem alkalmazható a gyógyszerkomponensekkel szemben túlérzékeny betegek, valamint a terhes és szoptató nők kezelésére. A bevacizumab terápia ellenjavallt gyermekeknél, valamint vese- és májelégtelenségben szenvedőknél, mivel a gyógyszer hatásosságát és biztonságosságát az ilyen betegekkel kapcsolatban nem igazolták. A fenti ellenjavallatok mindegyike releváns akkor is, ha ezt a gyógyszert szemészetben alkalmazzák.
Utasítások az Avastin alkalmazásához: módszer és adagolás
A gyógyszer intravénás injekciója szigorúan tilos, az Avastin injekciót csak intravénásan csepegtetheti. A szükséges koncentrátummennyiség 0,9% -os nátrium-klorid-oldat segítségével történő hígítása a szükséges térfogatra történik, miközben a sterilitás minden szabályát figyelembe vesszük. Az elkészített készítménynek bevacizumabot kell tartalmaznia 1,4-16,5 mg / ml tartományban. Az Avastin kezdeti adagját kemoterápia után, intravénás infúzió formájában adják be 90 percig, a következő dózisok alkalmazása kemoterápia után és előtt is lehetséges. Ha a beteg jól tolerálta az első infúziót, akkor a második bevezetésének ideje 60 percre csökken, és a pozitív reakciók fenntartása mellett az Avastin további infúzióit 30 percen belül végezzük. Nemkívánatos események esetén az Avastin alkalmazását teljesen vagy ideiglenesen fel kell függeszteni.
Normál adagolás
Metasztatikus vastagbélrák esetén:
- Első vonalbeli gyógyszerként: 5 mg / 1 kg testsúly 1 alkalommal 2 hét alatt, vagy 7,5 mg / 1 kg testsúly 1 alkalommal 3 hét alatt intravénásan, lassan.
- Másodlagos gyógyszerként 5-10 mg testtömeg-kilogrammonként kéthetente egyszer, intravénásan, lassan.
Helyileg visszatérő vagy áttétes emlőrák esetén 10 mg / testtömeg-kg, intravénásan, kéthetente egyszer, lassan.
Gyakori inoperábilis, visszatérő vagy áttétes nem laphámsejtes tüdőrák esetén az Avastin-t 7,5-15 mg / testtömeg-kilogramm adagban írják fel három hetente egyszer, attól függően, hogy milyen típusú kemoterápiát írnak fel a gyógyszer mellett.
Előrehaladott és / vagy áttétes vesesejtes karcinóma esetén a gyógyszert testtömeg-kilogrammonként 10 mg dózisban írják fel kéthetente egyszer, intravénásan, lassan.
A glioblastoma (IV. Fokozatú glioma) esetén az Avastint 10 mg / testtömeg-kilogramm dózisban írják fel kéthetente egyszer intravénásan, lassan.
A petefészek, a petevezeték hámrákjában, valamint a hashártya primer rákjában a gyógyszert három hetente egyszer, 15 mg / testtömeg-kilogramm dózisban írják fel intravénásan, lassan.
Első vonalbeli gyógyszerként az Avastint a karboplatin és a paklitaxel mellett írják fel, míg a kemoterápia maximális időtartama 6 ciklus, amely után az Avastin monoterápiát folytat.
A gyógyszer teljes kezelésének időtartama 15 hónap. Ha a betegség progressziójának tünetei megjelennek, az Avastin-kezelést nem szabad folytatni.
Daganat megismétlődése esetén az Avastin-t karboplatinnal és gemcitabinnal kombinálva írják fel (6-10 ciklus), majd a gyógyszert monoterápiaként alkalmazzák.
Mellékhatások
Az Avastin áttekintése azt jelzi, hogy a legsúlyosabb mellékhatások a gyomor-bél traktus perforációja, vérzés, beleértve a tüdővérzést vagy a hemoptysis, valamint az artériás thromboembolia formájában jelentkeznek. Emellett gyakran talál panaszokat magas vérnyomás, hasmenés, hasi fájdalom, gyengeség vagy aszténia miatt. Az Avastinra vonatkozó utasításokban az említetteken kívül a gyógyszer beadásával kapcsolatos mellékhatások következő lehetséges megnyilvánulásait jelzik:
- Fokozott vérnyomás, artériás tromboembólia, mélyvénás trombózis, pangásos szívelégtelenség, vérzés;
- Neutropenia, leukopenia, lázas neutropenia, thrombocytopenia, anaemia;
- Székrekedés, hasmenés, hányás, hányinger, végbélvérzés, étvágytalanság, szájgyulladás;
- Bélelzáródás, emésztőrendszeri rendellenességek, hasi fájdalom, a gyomor-bél traktus perforációja;
- Rhinitis, orrvérzés, légszomj, hipoxia, tüdő tromboembólia;
- Száraz bőr, elszíneződés, hámló dermatitis, tenyér-plantáris szindróma;
- Fokozott könnyezés, károsodott vizuális funkció;
- Arthralgia, myalgia, izomgyengeség;
- Proteinuria, húgyúti fertőzés;
- Asthenia, láz, fokozott fáradtság, különböző lokalizációjú fájdalom, tályog, kiszáradás, szepszis.
Csökkenthető a hemoglobin szintje, a hiperglikémia, a leukopenia, a hypokalemia, a thrombocytopenia is.
Túladagolás
Az Avastin intravénás adagolása 2 hetente maximum 20 mg / kg dózisban bizonyos esetekben súlyos fejfájást (migrént) észlel. A túladagolás fokozott mellékhatásokhoz is vezethet, amelyek dózisfüggőek. Nincs specifikus ellenszer, ezért tüneti kezelést végeznek.
Különleges utasítások
Az Avastin-kezelés ideje alatt és azt követően legalább hat hónappal a fogamzóképes korú nőknek és férfiaknak megbízható fogamzásgátlókat kell használniuk. Az összes szükséges információ utasításainak tartalma ellenére a kinevezést, az oldat elkészítését és adagolását csak tapasztalt szakorvos végezheti.
A bevacizumab gyógyszerészeti jellemzői nem kompatibilisek a dextróz oldattal.
Alkalmazás terhesség és szoptatás alatt
A terhesség és a szoptatás ellenjavallat az Avastin kinevezésében. A reproduktív korú férfiaknak és nőknek nyomatékosan ajánlott megbízható fogamzásgátló módszerek alkalmazása a gyógyszeres terápia alatt és a kezelés befejezése után legalább 6 hónapig.
Az Avastin termékenységi problémákhoz vezethet a nőknél. A legtöbb betegben a termékenység a gyógyszer megvonása után helyreáll. A gyógyszeres kezelés termékenységre gyakorolt hatása szempontjából hosszú távú következményei továbbra sem ismertek. A gyógyszeres terápia során és annak befejezését követően legalább 6 hónapig le kell állítani a szoptatást.
Alkalmazása időseknél
Az Avastin-t óvatosan írják fel idős (65 év feletti) betegek számára.
Gyógyszerkölcsönhatások
Klinikai tanulmányok bizonyítják, hogy az Avastin és kemoterápiás tanfolyamok kombinációja gyakorlatilag nincs hatással a gyógyszer farmakokinetikájára. Klinikailag vagy statisztikailag szignifikáns különbségek a gyógyszer clearance-ben a monoterápiában részesülő betegeknél és azoknál a betegeknél, akiknél az Avastin-t interferon alfa-2a-val vagy más kemoterápiás gyógyszerekkel (ciszplatin / gemcitabin, FU / LV, IFL, doxorubicin, kapecitabin, karboplatin) kombinációban alkalmazták / paclitaxel) nem azonosították.
A gyógyszer alkalmazása nem befolyásolja az irinotekán és aktív metabolitja (SN38), a ciszplatin, a kapecitabin és metabolikus termékei, az alfa-2a-interferon, az oxaliplatin farmakokinetikai tulajdonságait (az összes és szabad platina-tartalom alapján meghatározva). Nincsenek megbízható adatok az Avastin gemcitabin farmakokinetikájára gyakorolt hatásáról.
Ha a gyógyszert 2 hetente egyszer 10 mg / kg dózisban és a szunitinibet (50 mg naponta) kombinálják metasztatikus vesesejtes karcinómában szenvedő betegeknél, néha mikroangiopátiás hemolitikus vérszegénység eseteit észlelik, amelyek thrombocytopenia, vérszegénység és az eritrociták töredezettsége formájában nyilvánulnak meg. Elszigetelt esetekben a betegek artériás hipertóniában is szenvednek, beleértve a magas vérnyomású krízist, az emelkedett kreatininszintet és a neurológiai rendellenességeket. Ezek a tünetek reverzibilisek és szinte eltűnnek a szunitinib és a bevacizumab kezelés abbahagyása után.
Ha az Avastint a sugárterápia és a kemoterápia (temozolomid) kiegészítéseként írják fel kezdetben diagnosztizált glioblastomában szenvedő betegeknél, a gyógyszer biztonsági profilja nem változik.
Az Avastin hatékonysága és biztonságossága a sugárterápia kiegészítéseként más javallatok esetén nem bizonyított. A gyógyszer figyelemre méltó a dextróz oldatokkal való gyógyszerészeti összeférhetetlenség miatt.
Analógok
Az Avastin analógjai, amelyek hatásmechanizmusában szorosak és egy farmakológiai alcsoportba tartoznak, a következők: Vectibix, Herceptin, Campas, Mabthera, Erbitux, Arserra, Removab, Perieta, Herceptin liofilizátum, Rituximab, Acellbia, Mabtera.
A hatóanyagnak nincsenek a gyógyszer analógjai.
A tárolás feltételei
Az Avastint sötét helyen, 2-8 ° C hőmérsékleten kell tárolni. A kész oldatot napközbeni használatra alkalmasnak tartják.
A gyógyszertárakból történő kiadás feltételei
Vény alapján kiadva.
Vélemények az Avastinról
A vélemények szerint az Avastin különböző módon hat a szervezetre. Sok beteg állapotának jelentős javulásáról és a daganat méretének csökkenéséről számol be, de a teljes gyógyulás szinte lehetetlen. Emellett a betegek gyakran panaszkodnak a gyógyszer mellékhatásaira: vérnyomás-emelkedésre, fejfájásra és esetenként látásromlásra a teljes vakságig. Nem vonzza őket a gyógyszer magas költsége.
Az Avastin ára a gyógyszertárakban
Az Avastin (1 üveg 16 ml) hozzávetőleges ára átlagosan 22 050-24 500 rubel.
Avastin: árak az online gyógyszertárakban
|
Gyógyszer neve Ár Gyógyszertár |
|
Avastin 100 mg / 4 ml koncentrátum infúziós oldat elkészítéséhez 4 ml 1 db. 8755 RUB megvesz |
|
Avastin 400 mg / 16 ml koncentrátum infúziós oldat elkészítéséhez 16 ml 1 db. 36 770 rubel megvesz |

Maria Kulkes orvosi újságíró A szerzőről
Iskolai végzettség: I. M. az első moszkvai állami orvosi egyetem Szecsenov, az "Általános orvoslás" szakterület.
A gyógyszerről szóló információk általánosak, csak tájékoztató jellegűek, és nem helyettesítik a hivatalos utasításokat. Az öngyógyítás veszélyes az egészségre!